Fórmula De La Densidad – Conoce Los 4 Tipos De Densidad!
Las distintas partículas que en la naturaleza existen, se encuentran conformadas por partículas (moléculas, átomos o iones) que dado las condiciones de presión y de temperatura a las que se encuentran van a definir el estado de agregación molecular (líquido, sólido o gaseoso) y una condición que es muy característica. Para lograr determinar el estado tan singular de la sustancia, se utiliza la propiedad física intensiva llamada densidad (ρ), la cual nos indicara la cantidad de masa del cuerpo material que se encuentra contenido en un definido volumen de ella. Sigue leyendo y averigua la fórmula de la densidad, la historia, los tipos de densidades y la medición.
Fórmula de la densidad.
En química y en física, es la densidad una magnitud escalar la cual es referida a la cantidad de masa en un volumen determinado de una sustancia. Se simboliza usualmente por medio de la letra rho “ρ” del alfabeto griego. Es la densidad media la relación que existe entre la masa de un cuerpo y el volumen que este ocupa. Y la fórmula de la densidad es la siguiente:
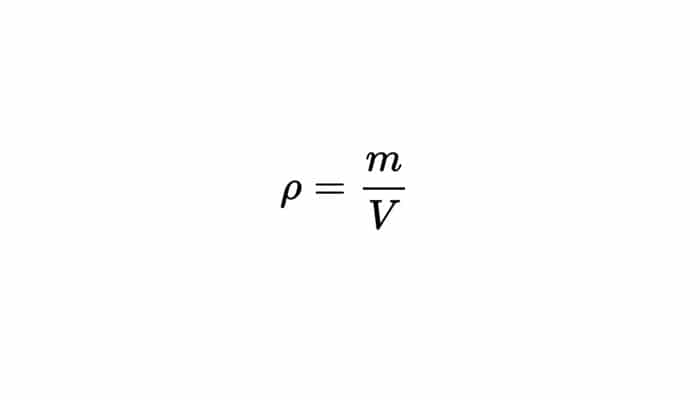
Si un cuerpo no posee una uniforme distribución de la masa en todos sus puntos, la densidad alrededor de algún punto dado puede discrepar de la densidad media. Si se supone una sucesión de pequeños volúmenes decrecientes ∆Vk (aproximándose hacia un volumen muy pequeño) concentrados alrededor de un punto, siendo ∆mk la masa que está contenida en cada uno de los volúmenes anteriores, entonces la densidad en el punto común a todos los volúmenes es:
 La Bandera De Inglaterra - Conoce Las Banderas Del Reino Unido!
La Bandera De Inglaterra - Conoce Las Banderas Del Reino Unido!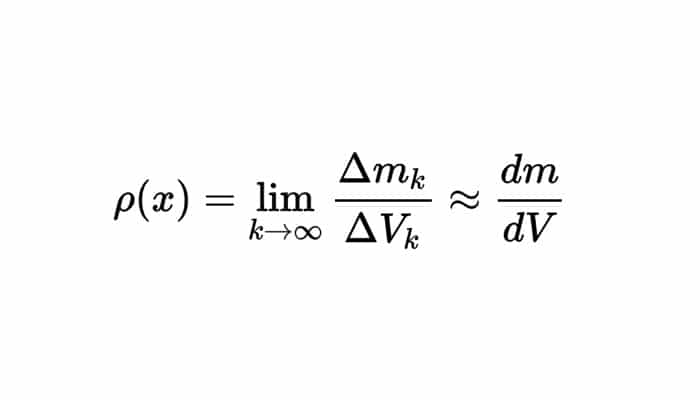
Ya que hemos denotado la fórmula de la densidad se debe tener en cuenta lo siguiente:
- Dependen los valores de densidad de las sustancias, de la temperatura y la presión a la cual se encuentre, aunque no dependen de la gravedad; por tal razón, la densidad de un cuerpo en la tierra es prácticamente igual que en la luna, a la misma presión y misma temperatura.
- Estando a igual presión y temperatura es posible diferenciar a dos químicamente sustancias puras, esto por sus valores de densidad, prácticamente esto se debe a que es una propiedad intensiva y además característica de cada sustancia.
- Se cumple para una sustancia química, generalmente: Dsólido > Dlíquido > Dgas
- varía en cantidades muy pequeñas la densidad de sustancias liquidas y sólidas con la temperatura, por lo cual se considera generalmente constante en un nivel de temperatura de 0°C a 30°C. Se debe considerar en cálculos muy precisos que la densidad minimiza al aumentar la temperatura, se debe esto a la dilatación o aumento de volumen que las sustancias experimentan al ser calentadas.

Interesante artículo: Averigua Quien Inventó El Microscopio Y Por Qué Es Importante Este Instrumento!
 7 Ventajas De La Energía Nuclear - Renovable O No Renovable
7 Ventajas De La Energía Nuclear - Renovable O No RenovableHistoria de la densidad.
Luego de haber sabido que es la densidad y la fórmula de la densidad, empecemos a tocar la historia. Según una muy conocida anécdota, recibió Arquímedes el encargo de poder determinar si el orfebre de Hierón II de Siracusa desfalcaba el oro durante la elaboración de una corona que era dedicada a los dioses, sustituyéndolo por algún otro metal más barato (proceso que es conocido como aleación). Sabía Arquímedes que la corona en un estado de forma irregular, podría ser aplastada o fundida en un cubo para que su volumen se puede calcular fácilmente comparado con la masa. Aunque el rey no estaba de acuerdo con tales métodos, ya que habrían supuesto la destrucción de la corona.
Se dio Arquímedes un relajante baño de inmersión, y el observando la subida del agua caliente cuando él permanecía en ella, descubrió en ese momento que podía calcular el volumen de la corona de oro por medio del desplazamiento del agua. Hallado pues el volumen, se podía multiplicar por la densidad del oro, encontrando el peso que debiera poseer si fuera de oro puro (es muy alta la densidad del oro, de 19 300 kg/m³, y pues cualquier otro metal, que esté aleado con él, la tiene menor), posteriormente si el peso no fuera el que perteneciera a si fuera de oro, significaba esto que la corona tendría aleación de algún otro metal.
Supuestamente, cuando Aristóteles hizo este descubrimiento salió corriendo desnudo por las calles mientras gritaba: “¡Eureka! ¡Eureka!” (En griego significa: “Lo encontré”). Entonces como resultado, el término “Eureka” ingresó en el lenguaje común, y se usa hoy día para indicar un momento de iluminación.
Apareció la historia por primera vez de manera escrita en De Architectura de Marco Vitruvio, luego de dos siglos luego de que supuestamente tuviese lugar. Aunque, algunos estudiosos han dudado de la veracidad de tal relato, afirmando (entre otras cosas) que dicho método habría exigido medidas exactas las cuales habrían sido difíciles de realizar en ese momento.
Dice otra versión de la historia que notó Arquímedes que experimentaba un empuje hacia arriba al encontrarse sumergido en el agua, y luego pensó que, pesando la corona, sumergida en agua, y poniendo en el otro platillo de la balanza el mismo peso en oro, sumergido también, la balanza estaría equilibrada si la corona era de oro efectivamente. El empuje hacia arriba del agua ciertamente, sería igual si en los dos platillos se encontraban objetos del mismo volumen y del mismo peso. Con ello, la dificultad de lograr conocer con exactitud el volumen de un sólido de forma irregular, en la época, se dejaba pues de lado. Nació de esta otra versión la idea del principio de Arquímedes.
Nació mucho más tarde, entre los científicos el concepto de densidad, en los tiempos en que las unidades de medida eran diferentes en cada país, de manera que, para evitar expresarlo en términos de las diferentes unidades de medida usuales para cada cual, determinaron a cada materia un número adimensional, que prácticamente era la relación entre la masa de tal materia y la de un volumen que es igual de agua pura, sustancia que se hallaba en cualquier laboratorio (densidad relativa). Cuando se determinó la unidad de peso en el sistema métrico decimal, el kilogramo (kg), como un decímetro cúbico (o sea un litro), de agua pura, la cifra utilizada hasta entonces, logró coincidir con la densidad absoluta (eso si se mide en kilogramos por litro, unidad de volumen en el antiguo Sistema Métrico Decimal, pero aceptada por el SI, y no en kilogramos por metro cúbico, que es pues la unidad de volumen en el SI).
Debes saber sobre los: Interesantes Cromosomas Del Ser Humano… ¡Lo Que Debes Saber De Tus Células!
Los tipos de densidad.
La densidad absoluta.
La densidad o llamada también densidad absoluta es pues la magnitud que expresa la relación hay entre el volumen y la masa de una sustancia. Es su unidad en el Sistema Internacional (SI) kilogramo por metro cúbico (o sea kg/m³), no obstante frecuentemente es también expresada en g/cm³. Es la densidad una magnitud intensiva.
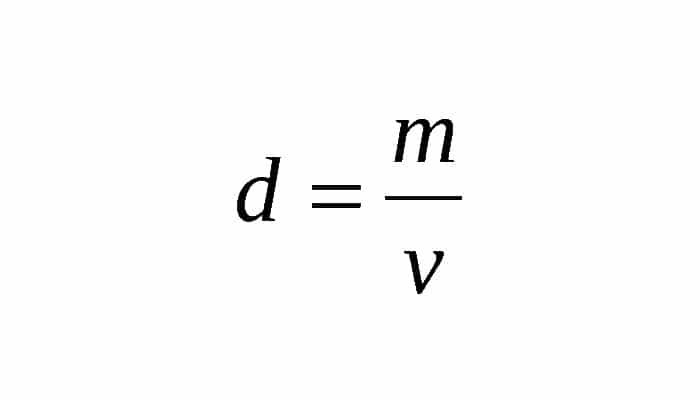
Siendo d, la densidad; V, el volumen; y m, la masa de la sustancia.
Densidad relativa.
La densidad relativa viene siendo la comparación de la densidad de una sustancia con la densidad de otra, la cual se toma como referencia. Se expresan ambas densidades en las mismas unidades y en idénticas condiciones de presión y temperatura. Es adimensional la densidad relativa (o sea sin unidades), esto porque queda definida como el cociente de dos densidades.
En ocasiones se le llama densidad específica (en inglés: specific density) en especial en los países con una fuerte influencia anglosajona. Es incorrecta tal denominación, por cuanto que el término “específico” en ciencia significa por unidad de masa. Bien, se detalla la densidad relativa como aquella razón que hay entre la densidad que es de una sustancia primordialmente y la de otra sustancia que es tomada como referencia, dando pues como resultado:
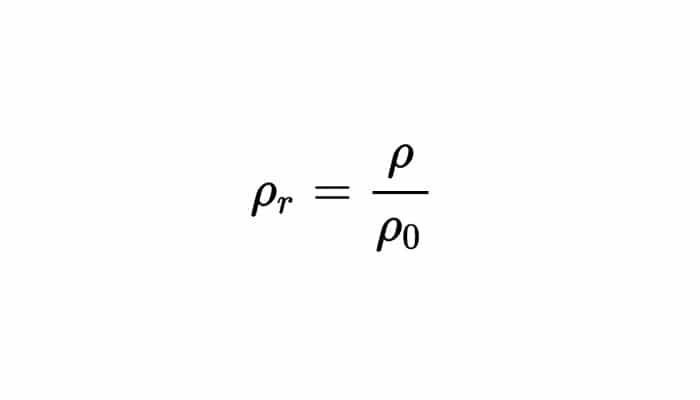
Donde ρr viene siendo la densidad relativa, ρ la densidad de la sustancia, y ρ0 es la densidad de referencia o la densidad absoluta.
Para los sólidos y los líquidos, la densidad usual de referencia es la del agua líquida a la presión de 1 atm, en tanto que la temperatura de 4 °C. Es en tales condiciones, la densidad absoluta del agua destilada de 1000 kg/m³, eso quiere decir, 1 kg/dm³.
La densidad de referencia habitual para los gases, es la del aire a una temperatura de 0 °C y a la presión de 1 atm.
Se puede también medir o calcular la densidad relativa como el cociente que existe entre los pesos o masas de los volúmenes idénticos de la sustancia problema y también de la sustancia de referencia:
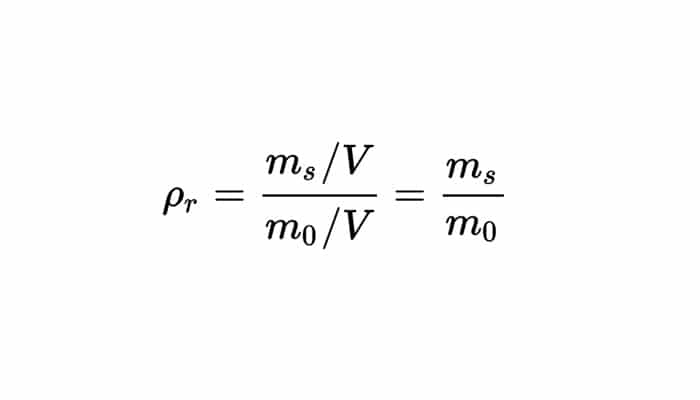
Densidad media y densidad puntual.
La expresión masa/volumen para un sistema homogéneo, se puede aplicar en cualquier región del sistema logrando siempre el mismo resultado.
Aunque, no presenta la misma densidad en diferentes partes un sistema heterogéneo. Hay que medir en este caso, la “densidad media”, dividiendo la masa del objeto por su propio volumen o la “densidad puntual” que será diferente en cada posición, punto o porción “infinitesimal” del sistema, y por lo tanto vendrá definida por:
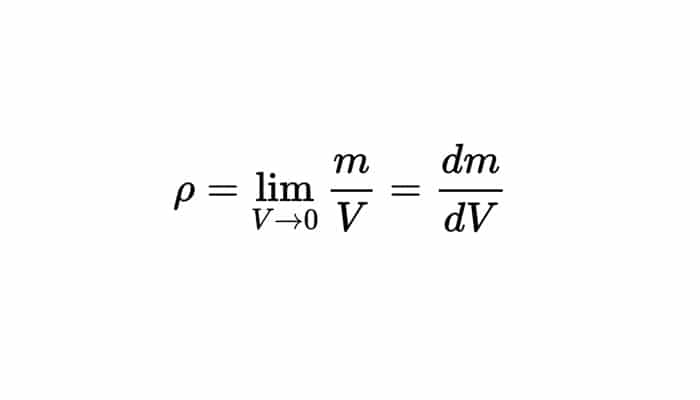
Aunque, debe tener en cuenta que las hipótesis de la mecánica de medios continuos son solo válidas hasta escalas de 10-8 m, esto porque a escalas atómicas la densidad no se encuentra bien definida. Por ejemplo, es cerca de 10-13 m el tamaño del núcleo atómico y se concentra en él la inmensa mayor parte de la masa atómica, por lo que su densidad (2,3·1017 kg/m3) es bastante superior a la de la materia ordinaria, o Sea, a una escala atómica dista la densidad mucho de ser uniforme, ya que están esencialmente vacíos los átomos, con prácticamente toda la masa reunida en el núcleo atómico.
Densidad aparente.
Es la densidad aparente una magnitud que es aplicada en materiales que tienen constitución heterogénea, y entre ellos, los porosos como lo es el suelo, los cuales conforman cuerpos heterogéneos con intersticios de aire o alguna otra sustancia, de manera que la densidad total de un volumen del material es pues menor que la densidad del material poroso si este se compactase. Se tiene en el caso de un material mezclado con aire:
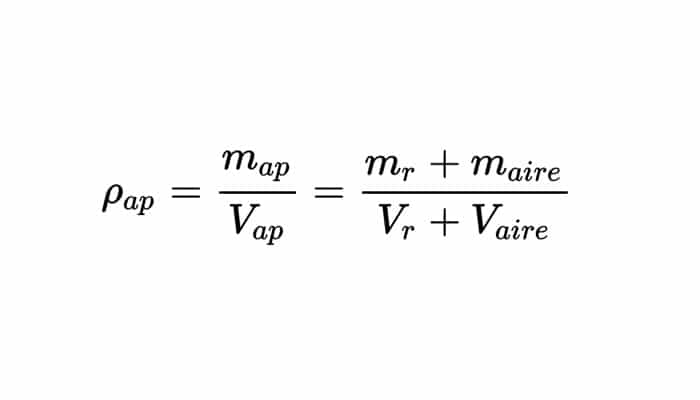
No es una propiedad intrínseca del material, la densidad aparente de un material y esta depende de su compactación. Se obtiene la densidad aparente del suelo (ρap) extrayendo una muestra de suelo de un conocido volumen a 105 °C incluso peso constante.
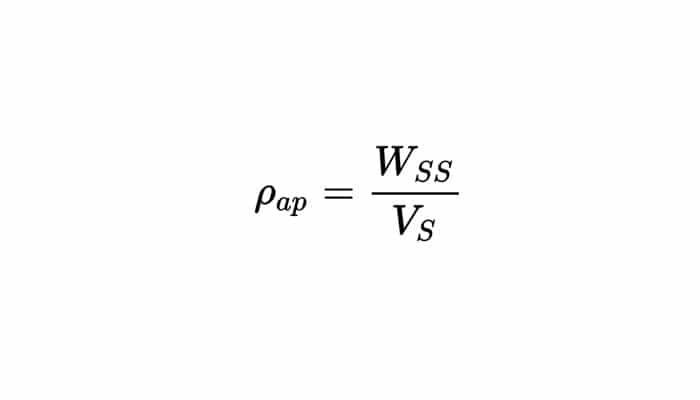
Dónde:
WSS, es el peso de suelo secado a 105 °C incluso peso constante.
VS, es el volumen original de la muestra de suelo.
También se debe considerar que para las muestras de suelo que varíen su volumen cuando se estén secando, como son los suelos con alta concentración de arcillas 2:1, se tiene que expresar el contenido de agua que tenía la muestra al instante de tomar el volumen.
Se considera en construcciones la densidad aparente de elementos usados en la obra, como por ejemplo de un muro hecho de ladrillo, que contiene mortero de cemento o de yeso, ladrillos y huecos con aire (cuando es el ladrillo hueco o perforado).
Medición de la densidad.
Puede la densidad obtenerse de forma directa y de forma indirecta. Se miden para la obtención indirecta de la densidad, el volumen y la masa por separado y luego se calcula la densidad. Habitualmente la masa es medida con una balanza, en tanto que puede medirse el volumen determinando la forma del objeto y calculando las dimensiones apropiadas o por medio del desplazamiento de un líquido, entre otros diferentes métodos. Son los instrumentos más comunes para medir la densidad:
- El picnómetro, este instrumento permite la medida precisa de la densidad de líquidos, sólidos y gases (picnómetro de gas).
- El densímetro, el cual permite la medida directa de la densidad, pero la de un líquido.
- La balanza de Mohr (variante además de balanza hidrostática), que admite la medida precisa de la densidad de los líquidos.
- La balanza hidrostática, permite este instrumento calcular densidades de sólidos.
Otra posibilidad para lograr determinar las densidades de los líquidos y de los gases es usar un instrumento digital, es cual es basado en el principio del tubo en U oscilante. Cuya frecuencia de resonancia se encuentra determinada por los materiales contenidos, como lo es la masa del diapasón es concluyente para la altura del sonido.

Importante que sepas acerca de las: Desventajas De La Energía Nuclear Y Sus Aplicaciones Bélicas!
Las unidades para la densidad.
Las unidades de medida más utilizadas en el Sistema Internacional de Unidades (SI) son:
- Gramo por mililitro (g/mL), que es equivalente a (g/cm³).
- Kilogramo por metro cúbico (kg/m³).
- Gramo por centímetro cúbico (g/cm³).
- kilogramo por decímetro cúbico o Kilogramo por litro (kg/L). Es la densidad del agua aproximadamente de 1 kg/L (1000 g/dm³ = 1 g/mL = 1 g/cm³).
- Suele usarse para los gases el gramo por litro (g/L) o gramo por decímetro cúbico (g/dm³), con la finalidad de facilitar con la constante universal de los gases ideales:
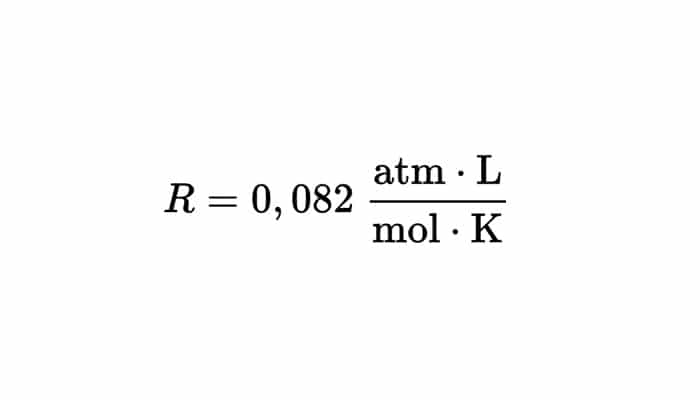
Cambios de densidad.
La densidad de una sustancia que en general, varía cuando cambia la temperatura o la presión, y también en los cambios de estado. Se ha establecido en particular empíricamente:
- Cuando incrementa la presión, también aumenta la densidad de cualquier material estable, notablemente en los gases, casi inapreciable en los líquidos y sólidos.
- Al aumentar la temperatura como regla general, la densidad decrece (si permanece constante la presión). Aunque, hay notables excepciones a esta regla. Por ejemplo, la densidad del agua dulce sube entre el punto de fusión (o sea a 0 °C) y los 4 °C; algo parecido ocurre con el silicio a temperaturas bajas.
Es muy pequeño el efecto de la presión y la temperatura en los líquidos y sólidos, por lo que típicamente la compresibilidad de un sólido o líquido es de 10−6 bar−1 (1 bar=0,1 MPa) y es de 10−5 K−1 el coeficiente de dilatación térmica. Las anteriores consideraciones llevan a que una ecuación de estado para alguna substancia ordinaria, debe lograr satisfacer las restricciones siguientes:
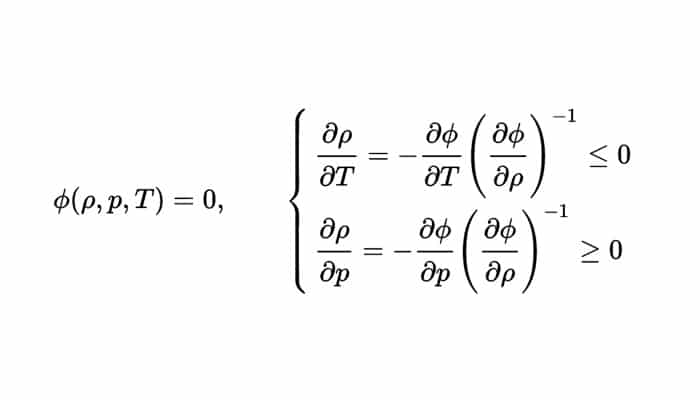
La densidad de los gases por otro lado, se observa notablemente afectada por la temperatura y la presión. Describe matemáticamente la ley de los gases ideales la relación que hay entre estas tres magnitudes:
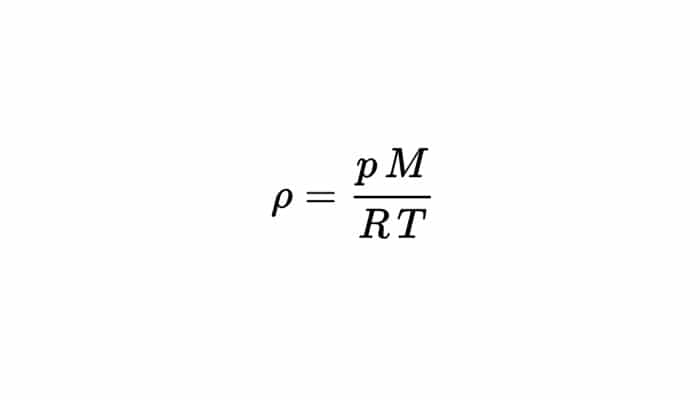
Donde p es la presión del gas, R es la constante universal de los gases ideales, T la temperatura absoluta y M su masa molar. Significa eso que un gas ideal a 27 °C (300 K) y 1 atm duplicará su densidad si se incrementa la presión a 2 atm manteniendo constante la temperatura o, alternativamente, se minimiza su temperatura a 150 K manteniendo constante la presión.

No dejes de saber sobre: Los Inventos De Albert Einstein – Desde Teorías Hasta Un Refrigerador!
Si quieres conocer otros artículos parecidos a Fórmula De La Densidad – Conoce Los 4 Tipos De Densidad! puedes visitar la categoría Ciencia Y Cultura.
Deja una respuesta
Buenas noches, tengo una consulta en relación con la densidad y las formulas. Si tengo el peso de una persona y además el área total de los pies ¿Cómo podré determinar su densidad?
Gracias 🙂